Zusammenfassung
Das vorliegende Werk bietet aktuelle evidenzbasierte Informationen zur Diagnose und Therapie von Störungen der chemischen Sinne Riechen und Schmecken für behandelnde HNO-Ärzte und -Ärztinnen sowie auch andere Fachgebiete, die mit diesen Beschwerden befasst sind, v.a. die Allgemeinmedizin und Neurologie, aber auch die Zahnheilkunde. Dabei wird auf gute Lesbarkeit sowie klinische Relevanz geachtet, um die klinische Anwendbarkeit zu garantieren.
Durch die COVID-19-Pandemie ergibt sich durch die damit einhergehende Häufung von Patient:innen mit Riechstörungen eine zusätzliche Relevanz.
Leseprobe
Inhaltsverzeichnis
Die spezialisierte Riechschleimhaut befindet sich im Dach beider Nasenhaupthöhlen. Die Regio olfactoria erstreckt sich im Bereich der oberen Nasenmuschel bis zum Ansatz der mittleren Nasenmuschel und der gegenüberliegenden Nasenscheidewand. Das Riechepithel ist im Prinzip aus drei Zellarten aufgebaut. Erstens aus den eigentlichen Riechnervenzellen (ORN, olfaktorische Rezeptorneurone), die auf den mikroskopisch kleinen, in den Schleim der Nasenhöhle ragenden Zellfortsätzen (Mikrovilli) Duftstoffrezeptoren tragen. Zweitens aus den Stützzellen, die die Riechnervenzellen umgeben und für deren regelrechte Funktion mitverantwortlich sind. Der dritte Zelltyp der Riechschleimhaut sind die Basalzellen (Reservezellen, pluripotente Stammzellen), von denen die ständige Regeneration der Riechnervenzellen ausgeht. Dies ist eine Besonderheit des menschlichen Körpers, da normalerweise zugrunde gegangene Nervenzellen nicht ersetzt werden. Dadurch erklärt sich auch die Regenerationsfähigkeit bei nerval bedingten Riechstörungen.
Das Axon der Riechnervenzelle verläuft durch die Lamina cribrosa des Siebbeins gemeinsam mit anderen Axonen als Fila olfactoria. Sie bilden gemeinsam den ersten Hirnnerv (N. olfactorius). Die Riechnerven enden im Riechkolben (Bulbus olfactorius), der bereits einen Teil des Gehirns darstellt. Da die erste synaptische Umschaltung der Riechnerven erst im Riechkolben stattfindet, liegt somit über die Riechnervenzellen im menschlichen Körper eine direkte Verbindung der Außenwelt (Einatemluft) mit dem Zentralnervensystem vor.
Vom Riechkolben erfolgt die weitere Übertragung der Duftstoffsignale bis zur bewussten Wahrnehmung in der Großhirnrinde über den Tractus olfactorius zu den ältesten Anteilen des Gehirns, dem entorhinalen und piriformen Kortex sowie dem Limbischen System mit dem Mandelkern und dem Hippocampus. Diese Areale sind für die emotionale Bewertung von Sinneseindrücken verantwortlich.
Der Hippocampus spielt auch eine wichtige Rolle für das Gedächtnis und die Erinnerung. Daher können Gerüche starke Emotionen und vegetative Symptome auslösen sowie blitzartig vergangene Erlebnisse aufleben lassen. Im Bereich der Großhirnrinde sind unterschiedliche Hirnanteile an der Geruchswahrnehmung beteiligt, v. a. das Stirnhirn, aber auch Anteile des Schläfen- und Scheitellappens.
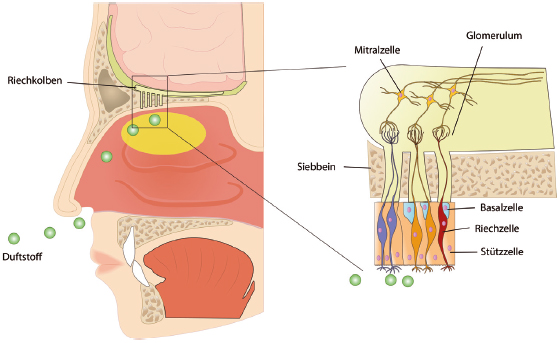
Abb. 1: Anatomie der Nasenhöhle mit Riechschleimhaut und Riechkolben. © ellepigrafica, Adobe Stock
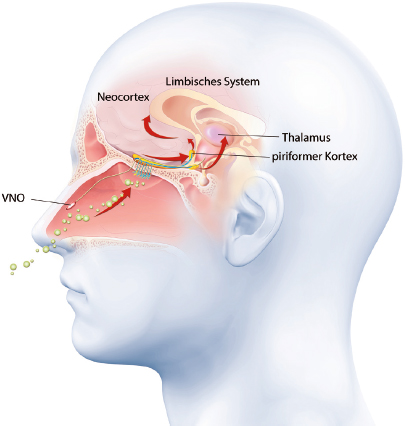
Abb. 2: Das erste Gehirnareal nach dem Riechkolben, das Informationen von Duftstoffen weiterverarbeitet, ist das Limbische System, danach wird die Großhirnrinde erreicht. Der Thalamus („Tor zum Bewusstsein“) wird nur teilweise in die Verarbeitung der Duftstoffe einbezogen. Das Vomeronasalorgan (VNO) ist beim Menschen funktionslos. © Axel Kock, Adobe Stock
Der Weg der Duftstoffe ins Nasendach
Damit Gerüche überhaupt wahrgenommen werden können, müssen sie erst an die Riechschleimhaut transportiert werden. Dies geschieht mit dem Luftstrom sowohl beim Einatmen (und Schnüffeln) von vorne als auch beim Ausatmen (und Kauen, Schlucken) von hinten. Der Hauptluftstrom passiert dabei die unteren Nasenbereiche (v. a. untere Nasenmuschel, unterer Nasengang) und nur ein kleinerer Teil gelangt durch Verwirbelungen nach oben ins Nasendach. Bereits durch kleine Veränderungen der Anatomie der Nase und der Nebenhöhlen sowie der Schleimhaut selbst (z. B. durch Schwellung, Austrocknung, Borkenbildung) kann es zu einer deutlichen Veränderung der Geruchswahrnehmung kommen.
Die wichtigsten für die Wahrnehmungsstärke von Duftstoffen verantwortlichen Variablen sind neben der Konzentration des Duftstoffs auch die Dauer und die Geschwindigkeit der Luft bei der Einatmung. Dabei hat sich im Studiendesign gezeigt, dass die langsame Einatmung die stärkste Empfindung auslöst.
Etwa 350 Duftstoffrezeptoren sind auf viele Millionen Riechnervenzellen der Riechschleimhaut verteilt, wobei jede Riechzelle einen spezifischen Rezeptor exprimiert. Sie werden von der größten zusammenhängenden Genfamilie des menschlichen Genoms codiert, die etwas mehr als ein Prozent aller Gene ausmacht. Es handelt sich um G-Protein-gekoppelte Rezeptoren, die bei konstanter Einwirkung von Geruchsmolekülen zur Adaptation beitragen. Dadurch übertragen die Riechnervenzellen trotz Vorliegen des Duftstoffs keine vermehrten Signale ins Gehirn. Außerdem kommt es im Riechkolben und im piriformen Kortex zur Adaptation durch inhibitorische Nervenzellaktivität. Der zweite Mechanismus, der zu einer abnehmenden bewussten Wahrnehmung von Duftstoffen beiträgt, liegt in komplexen multineuronalen unterdrückenden Rückkopplungsmechanismen im Gehirn, die als Habituation bezeichnet werden.
Wie können wir mit 350 verschiedenen Rezeptoren eine Vielzahl unterschiedlicher Gerüche wahrnehmen? Die Schätzungen der vom Menschen theoretisch unterscheidbaren Duftstoffe gehen in die Millionen. Dies wird durch die Kombination der Rezeptoren erreicht. Jeder Duftstoff kann mehrere Rezeptoren anregen, wodurch ein spezifisches „Bild“ oder eine „Geruchslandkarte“ (olfactory map) entsteht. Da auch jeder Rezeptor verschiedene Duftstoffe binden kann, ergibt sich dadurch eine riesige Anzahl möglicher Kombinationen von Erregungsmustern durch Gerüche. Die erste Verarbeitungsstation im Gehirn stellt der Riechkolben dar. Hier konvergieren alle Riechnervenfasern der 350 einzelnen Rezeptortypen auf jeweils eine mikroskopische Struktur, die als Glomerulum bezeichnet wird. Dort erfolgt die erste Umschaltung der primären olfaktorischen Rezeptorneurone über den synaptischen Neurotransmitter Glutamat auf die Mitralzellen, die über den Tractus olfactorius weiter zentral verlaufen.
Der physiologische Zellzyklus in der Riechschleimhaut läuft kontinuierlich von den Basalzellen in Richtung adulter Riechnervenzellen ab. Da dieser Zyklus mehrere Monate beträgt, ergibt sich bei Schädigung der Riechschleimhaut durch unterschiedliche Noxen die oft beobachtete lange Regenerationszeit. Außerdem kann die Regeneration nur erfolgen, sofern die Basalzellen nicht irreversibel geschädigt werden. Zusätzlich erschwerend kommt hinzu, dass neben der zellulären Erneuerung die komplexen Verläufe der Riechnerven durch das Siebbein im Bereich der Schädelbasis und deren Verschaltungen im Riechkolben wiederhergestellt werden müssen.
Die Riechschleimhaut als Eintrittspforte ins Gehirn
Aufgrund der Tatsache, dass die Riechnervenzellen eine direkte Verbindung der Umwelt mit dem Gehirn darstellen, kommt dem Schutz der Riechschleimhaut vor dem Einfluss toxischer und potenziell schädlicher Substanzen eine besondere Bedeutung zu. Folgende Mechanismen sind dafür verantwortlich:
1) die intrazelluläre Entgiftung schädlicher Substanzen,
2) die Bindung von Schadstoffen durch spezifische Proteine im Sekret der Riechschleimhaut,
3) die Zerstörung angegriffener Riechnervenzellen durch Zellen des Immunsystems und deren Ersatz durch die Basalzellen.
Sollten diese Mechanismen nicht ausreichend wirksam sein, ist es möglich, dass über die Riechschleimhaut Substanzen in das ZNS gelangen. Dafür stehen wiederum drei Möglichkeiten offen:
1) die direkte Aufnahme der Substanzen in die Riechnervenzellen und der Transport entlang des Axons zum Bulbus olfactorius (olfactory nerve pathway),
2) die perineurale Weiterleitung der Stoffe in den Subarachnoidalraum des Gehirns (olfactory epithelial pathway oder paracellular transport),
3) die Aufnahme von Substanzen in den Blutkreislauf aufgrund der ausgeprägten Durchblutung der nasalen Schleimhaut und der Riechschleimhaut (vascular pathway).
Eigenschaften von Duftstoffen
Welche Eigenschaften müssen Duftstoffe haben, damit sie wahrnehmbar sind? Die riechbaren Moleküle müssen flüchtig sein, d. h., die Fähigkeit besitzen, in die Gasphase überzutreten. Dies gelingt nur Molekülen mit einer maximalen atomaren Masse von ca. 300 Dalton, das entspricht etwa 20 Kohlenstoffatomen. Wenn Moleküle diese Masse übersteigen, dann benötigen sie zu viel Energie, um bei normaler Temperatur aus der freisetzenden Struktur herausgelöst werden zu können.
Entgegen früherer Annahmen belegen neuere Erkenntnisse, dass der menschliche Geruchssinn hervorragend ausgebildet ist. So können wir bestimmte Duftstoffmoleküle in deutlich geringeren Konzentrationen als so hervorragende Schnüffler wie die Mäuse wahrnehmen. Auch das Verfolgen von Duftspuren (scent tracking) in Analogie zu Fährtenhunden haben Menschen in Studien bewältigt. Dabei hat sich auch herausgestellt, dass die Ergebnisse durch ein Training verbessert werden können. Außerdem verwenden wir dabei zur besseren Lokalisation der Duftstoffe die minimal unterschiedlichen Informationen aus den beiden Nasenlöchern. Es kommt nämlich durch die zeitlich versetzte Erregung der Riechnervenzellen zu einer Seitendifferenz, die durch unser empfindliches olfaktorisches System detektiert werden kann. Werden dagegen durch passive Reizung beide Nasenlöcher gleichzeitig erregt, sodass in eine Nasenseite nur Luft und in die andere Seite ein Duftstoff-Luftgemisch geleitet wird, so haben Experimente gezeigt, dass die richtige Seite nicht korrekt erkannt werden kann. Diese Tatsache wird zur experimentellen Überprüfung der trigeminalen Eigenschaften von Duftstoffen ausgenutzt, da eine Lateralisation (die richtige Angabe der stimulierten Nasenseite) durch den N. trigeminus vermittelt wird.
Die falsche Tradierung über den schlechten menschlichen Geruchssinn begründet sich auf Einschätzungen von Freud und Broca, die nicht durch Experimente, sondern durch philosophische Annahmen begründet waren. So wurden die Primaten – und in weiterer Folge der Mensch – mit vermeintlich unterentwickeltem Geruchssinn den Tieren gegenübergestellt, deren Überleben von einem intakten Geruchssinn abhängt. Außerdem wurde dem Geruchssinn die vorrangige Bedeutung beim Sexualtrieb im Tierreich zugeschrieben und somit die Klassifizierung als „niederer Sinn“ beim „höher entwickelten“ Menschen festgeschrieben.
Feingeschmack
Dass beim plötzlich auftretenden Verlust des Riechvermögens ein wichtiger Teil unserer Wahrnehmung fehlt, bemerken die Betroffenen oft zuerst beim Essen und Trinken. Der Geruchssinn steuert über die retronasale Wahrnehmung der Aromen den Hauptbestandteil der sog. Feingeschmackswahrnehmung bei. Dabei gelangen die Duftstoffmoleküle der Speisen vom Mundraum durch Luftverwirbelungen beim Kauen und Schlucken über den Nasenrachen ins Dach der Nasenhöhle zur Riechschleimhaut. Im Gehirn wird dann über den N. trigeminus, der die Berührung im Mund vermittelt, der Duftstoff in den Mund „projiziert“ und wir „schmecken“ dann vermeintlich im Mund. Dies ist somit eigentlich eine trigeminal vermittelte Illusion. Fehlt nun der Anteil des Riechens beim Essen, schmeckt alles einheitlich, fad, ohne eigentliche Nuance. Man könnte den „Feinschmecker“ demnach auch als „Feinriecher“ bezeichnen.
Interessanterweise haben wir jedoch in einer eigenen Studie herausgefunden, dass ca. 10–15 % der Patient:innen mit komplettem Ausfall des Riechvermögens (Anosmie) nicht über Probleme mit dem Feingeschmack berichten. Dies verdeutlicht, dass die Wahrnehmung des Feingeschmacks eine kognitive Leistung aller fünf Sinne ist, deren einzelne Aspekte unterschiedlich zum Gesamterlebnis beitragen und auch teilweise ersetzt werden können. Neben der erwähnten Bedeutung des retronasalen Riechens und des N. trigeminus (vermittelt auch Temperatur und Konsistenz der Speisen) spielt auch der eigentliche Geschmackssinn (süß, sauer, salzig, bitter, umami) eine wichtige Rolle in der Feingeschmackswahrnehmung. Zu guter Letzt „isst man auch mit dem Auge“. Dies verdeutlicht die Beeinflussbarkeit unserer Sinneswahrnehmungen und erklärt die Schwankungsbreite der subjektiven Betroffenheit von Patient:innen mit Verlust des Geruchssinns.
Auch werden die Reaktionen auf Gerüche oder Präferenzen beim Essen großteils im Laufe unseres Lebens erlernt und können sich auch verändern. Gerade bei der Bewertung von Gerüchen während des Essens gibt es große individuelle und auch kulturelle Unterschiede. Manche Speisen werden von verschiedenen Personen ganz gegenteilig bewertet, je nachdem, wie und wann sie das erste Mal mit ihnen in Berührung gekommen sind. Man könnte daher auch sagen, dass wir primär nicht das essen, was uns schmeckt, sondern es schmeckt uns, was wir essen.
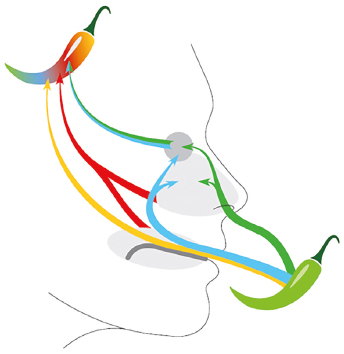
Abb. 3: Der Feingeschmack: Erst das Zusammenspiel aller Komponenten der chemischen Sinne (grün: orthonasales Riechen, blau: retronasales Riechen, gelb: Schmecken, rot: nasale und orale trigeminale Sensitivität) ergibt mit dem Seh- und Hörsinn das Gesamtbild der sensorischen Empfindung. Wir schmecken also mit allen Sinnen. © C. A. Müller & B. Renner
Warnfunktion
Der Geruchssinn hat auch die wichtige Funktion, uns vor Gefahren zu warnen. Untersuchungen haben gezeigt, dass sich die Wahrscheinlichkeit, Zwischenfälle aufgrund nicht wahrgenommener Gerüche zu erleiden, bei Anosmiker:innen verdoppelt. Darunter fallen Situationen beim Kochen (angebranntes Essen), die Einnahme bereits verdorbener Lebensmittel oder auch nicht wahrgenommener Gasgeruch oder Brandgeruch.
In der Beratung von Patient:innen mit Riechstörungen ist es daher wichtig, darauf aufmerksam zu machen. Insbesondere auf die Installation von Rauch- und Gasmeldern sollte hingewiesen werden.
Sozialfunktion
Der Körpergeruch beeinflusst die Interaktion zwischen den Menschen auf mehreren Ebenen. Einerseits nehmen wir unsere Mitmenschen bewusst über deren Geruch wahr. Wenn etwa Parfüm zu intensiv aufgetragen wird oder Schweißgeruch unangenehm auffällt, führt dies zu einer direkten Abwehrhaltung. Es ist daher bei Patient:innen mit Verlust des Riechvermögens darauf hinzuweisen, auf regelmäßige Körperhygiene zu achten.
Ebenso wichtig ist die unbewusste Kommunikation durch Gerüche. So konnte in Studien gezeigt werden, dass wir denjenigen:diejenige Partner:in unbewusst bevorzugt wählen, dessen:deren „genetischer Geruchsabdruck“ möglichst unterschiedlich von unserem eigenen ist. Damit kann für potenzielle Nachkommen eine möglichst hohe genetische Variabilität garantiert werden. Die Wahrnehmung des Körpergeruchs auf bewusster und unbewusster Ebene wird dabei über die Riechschleimhaut und nicht über das bei Tieren speziell ausgebildete Vomeronasalorgan (Wahrnehmung von Sexuallockstoffen/Pheromonen) vermittelt. Dieses hat beim Menschen keine Funktion und lässt sich lediglich als Blindsack ohne Nervenverbindung zum Riechhirn im Bereich der Nasenscheidewand nachweisen.
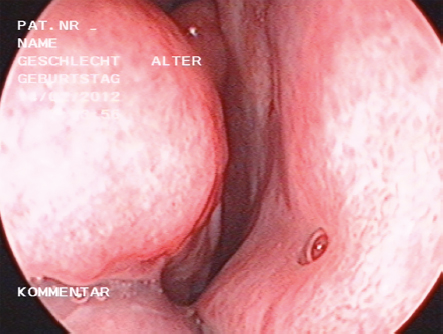
Abb. 4: Nasenscheidewand mit dem Rest des beim Menschen nicht funktionsfähigen Vomeronasalorgans (VNO), ein ca. 1 mm großes Grübchen im Bereich der vorderen Nasenscheidewand, das bei etwa einem Drittel der Menschen zu beobachten ist. © C. A. Müller, Meduni Wien
Lebensqualität
Der menschliche Geruchssinn hat einen wichtigen Anteil an unserer allgemeinen Lebensqualität. Neben den beschriebenen Bereichen, die etwa den Feingeschmack und die Warnfunktion betreffen, beklagen viele Patient:innen, erst mit dem Verlust des Geruchssinns einen wichtigen und oft unterschätzten Aspekt ihrer Sinneswahrnehmung verloren zu haben. So könne die Natur um sie herum nicht mehr wie gewohnt wahrgenommen werden. Viele Betroffene fühlen sich selbst „wie im Fernsehen“ und vermissen schmerzlich die verlorene Geruchsempfindung.
Untersuchungen haben ergeben, dass durch den Verlust des Riechvermögens viele Teilaspekte der Lebensqualität messbar abnehmen. Dies betrifft die Bereiche der Wahrnehmung beim Essen (Abnahme der Restaurantbesuche), aber auch soziale Bereiche wie die Abnahme von Sozialkontakten oder auch eine Veränderung des Sexuallebens.
Gesundheit
Ein weiterer interessanter Aspekt des Geruchssinns wurde in den letzten zehn Jahren beforscht. Dabei haben erste Studien einen möglichen Zusammenhang zwischen dem menschlichen Geruchssinn und der Mortalität gezeigt. So scheinen Personen mit einem ausgezeichneten Riechvermögen eine geringere Mortalität und somit eine längere Lebenswartung zu haben als Personen mit eingeschränktem Riechvermögen. Dieser Effekt wurde statistisch unabhängig von den das Riechvermögen beeinträchtigenden Erkrankungen gemessen, womit die Güte des Geruchssinns per se ein prognostischer Faktor für die Lebenserwartung sein könnte. Somit wären alle Maßnahmen, die zu einer Verbesserung des Riechvermögens beitragen, wie etwa ein Riechtraining, eine Investition in die Gesundheit. Einschränkend sei gesagt, dass der Effekt bei Personen im höheren Lebensalter untersucht wurde und noch nicht endgültig geklärt ist. Eine Erklärung für den Zusammenhang des Riechvermögens mit der Lebenserwartung wäre die Hypothese, dass die stetige Regeneration und die Funktion des hoch spezialisierten Riechepithels den prinzipiellen und allgemeinen Zustand der Regenerationsfähigkeit des Körpers widerspiegeln.
Die spezialisierten Geschmackszellen, die verschiedene Rezeptoren für die Geschmacksqualitäten süß, sauer, salzig, bitter und umami tragen, befinden sich vorwiegend auf der Zunge sowie im Bereich des weichen Gaumens und der Epiglottis. Die Geschmackszellen übertragen nach Reizung durch die spezifischen Geschmacksstoffe das Signal durch synaptische Übertragung auf periphere Neurone, sind selbst also im Unterschied zu den primären Riechneuronen keine Nervenzellen mit Weiterleitungsfunktion. Dadurch kann die Regeneration der Geschmackszellen deutlich schneller erfolgen. Die neben den fünf Basis-Geschmacksqualitäten der gustatorischen Wahrnehmung zugerechneten Empfindungen wie metallischer Geschmack, fettiger Geschmack oder Adstringenz (raues, pelziges Gefühl, z. B. durch Tannine in Wein und Tee hervorgerufen) werden durch orale Mechanorezeptoren auf freien Nervenendigungen der Schleimhaut vermittelt.
Zusammengefasst werden die spezialisierten Geschmackszellen in mikroskopischen Strukturen, den Geschmacksknospen (taste buds). Auf der Zunge befinden sich diese in den makroskopisch sichtbaren Geschmackspapillen (Zungengrund: Papillae circumvallatae/Wallpapillen, vordere Zunge: Papillae fungifomes/pilzförmige Papillen, Zungenrand: Papillae foliatae/blattförmige Papillen).
Bis auf den zentralen Bereich, der keine Geschmacksknospen enthält, können alle Areale der Zunge alle fünf Geschmacksqualitäten detektieren. Die in früheren Lehrbüchern tradierten Geschmackslandkarten beruhen auf falsch interpretierten Untersuchungsergebnissen von Hänig, der bereits im Jahr 1901 in seiner Dissertation „Zur Psychophysik des Geschmackssinnes“ die Empfindlichkeit der Zungenareale mittels Lösungen der damals bekannten vier Qualitäten nachwies. Die fünfte Qualität (umami) wurde erst 1908 vom Japaner Ikeda entdeckt und in weiterer Folge molekularbiologisch als Glutamatrezeptor nachgewiesen.
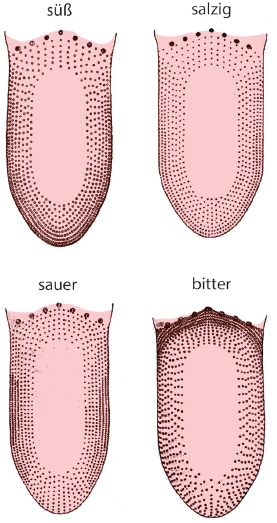
Abb. 5: Die Empfindlichkeit aller Zungenareale mit Geschmacksknospen für die Qualitäten süß, sauer, salzig und bitter konnte Daniel von Hänig in aufwendigen Untersuchungsreihen an Proband:innen nachweisen. Je dichter die Punkte angeordnet sind, desto empfindlicher zeigten sich die Areale. Nach D. P. Hänig, 1901, Zur Psychophysik des Geschmackssinnes. Leipzig.
Beteiligt an der gustatorischen Innervation sind drei Hirnnervenpaare (7., 9. und 10. Hirnnerv). Die Papillen der vorderen Zunge werden vom 7. Hirnnerv (N. facialis) innerviert und verlaufen peripher mit dem N. lingualis sowie im Bereich des Mittelohrs als Chorda tympani. Ebenfalls der 7. Hirnnerv versorgt die Geschmacksknospen des weichen Gaumens durch den N. petrosus major. Die hinteren Zungenareale werden durch den 9. Hirnnerv (N. glossopharyngeus) versorgt, die Epiglottis durch den 10. Hirnnerv (N. vagus).
Die gustatorischen Nervenbahnen der drei Hirnnervenpaare laufen im Hirnstamm über den Nucleus tractus solitarii zum Gehirn und projizieren auf den gustatorischen Kortex, der aus Insula und Operculum besteht.
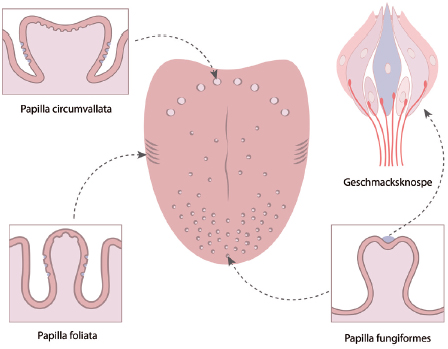
Abb. 6: Die drei Arten der Geschmackspapillen, die Geschmacksknospen ausbilden. Die für die Rauigkeit der Zunge verantwortlichen Papillae filiformes tragen keine Geschmacksknospen. © fancytapis, Adobe Stock
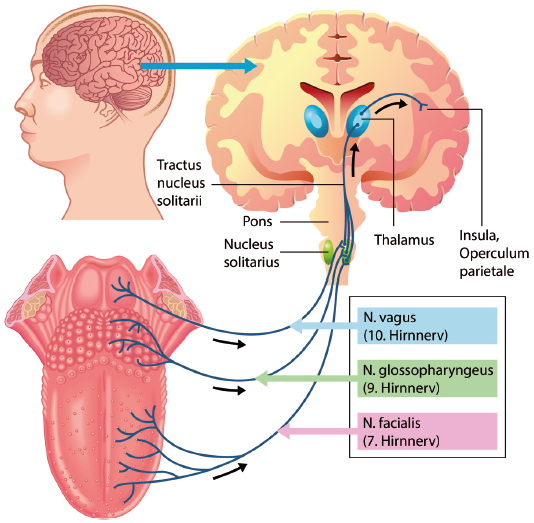
Abb. 7: Der Verlauf der Geschmacksbahn über den Hirnstamm bis zur Großhirnrinde. © rob3000, Adobe Stock
Die Transduktion der Sinnesreize erfolgt für die Geschmacksrichtungen süß, bitter und umami über G-Protein-gekoppelte Rezeptoren, für salzig und sauer über Ionenkanäle. So wird „sauer“ durch Blockade der Kaliumkanäle in der Zellmembran der Geschmackszellen durch H+-Ionen vermittelt. Dadurch kommt es zu einer verminderten Repolarisation durch K+-Ausstrom aus der Zelle und damit zu einer Depolarisation mit nachfolgender Neurotransmitterausschüttung. Ähnlich funktioniert salzig, wobei es hier anstelle einer H+-Blockade der K+-Kanäle zu einem direkten Einstrom von Natrium durch Na+- Kanäle und damit zur Depolarisation kommt.
Komplizierter gestaltet sich die Transduktion der G-Protein-gekoppelten Kanäle mit Verstärkerfunktion. So setzen Süß- und Bitterstoffe sowie Substanzen des Umami-Geschmacks (v. a. MSG, Monosodium Glutamate) eine Kaskade an intrazellulären Prozessen in Gang, die über sog. Second Messenger (cAMP) zu einer Phosphorylierung von Natriumkanälen und dadurch zu deren Öffnung und nachfolgender Depolarisation der Zelle führen. Dabei gibt es eine Vielzahl verschiedener Rezeptoren (v. a. bei der Bitter-Wahrnehmung, vermittelt durch T2R-Bitterrezeptoren), um auf chemisch unterschiedliche Liganden reagieren zu können.
Im Gehirn kommt es zur gegenseitigen zentralen Hemmung der vier Geschmacksareale auf der Zunge. Das bedeutet, dass die beiden vorderen, vom N. facialis innervierten Areale und die beiden hinteren, vom N. glossopharyngeus innervierten Areale bei Stimulation die Signale der jeweils anderen Region inhibieren. Somit kommt es bei Unterfunktion eines Areals zu einer Enthemmung (somit zur Verstärkung) der anderen Areale. Dies erklärt auch zum Teil, warum der Ausfall eines Areals (z. B. nach Durchtrennung der Chorda tympani bei Mittelohr-OP) nicht immer von den Patient:innen bemerkt wird.
Obwohl auf der Zungenmitte und auf der Wangenschleimhaut keine funktionellen Geschmacksknospen liegen, fühlen wir süß, sauer, salzig etc. im gesamten Mund. Das heißt, dass auch diese Areale Geschmacksempfindungen vermitteln. Möglich wird dies durch die Vermittlung des N. trigeminus. Analog zur Illusion des geruchsvermittelten Feingeschmacks im Mund (s. o.) ist auch dies eine Illusion durch die zentrale Interaktion der chemischen Sinne. Somit können auch durch diesen physiologischen Mechanismus Areale mit ausgefallener gustatorischer Sensitivität kompensiert werden.
Die Rolle des Speichels in der Geschmackswahrnehmung
Der Speichel besteht zu 99 % aus Wasser, wodurch die Geschmacksstoffe gelöst und zu den spezifischen Rezeptoren transportiert werden können. Nur 1 % des Speichels besteht aus anorganischen Ionen und organischen Molekülen. Na+, K+, Cl-, HCO3- sind die hauptsächlichen Ionen, die die konstante Hintergrundstimulation der Geschmacksrezeptoren ausmachen. Die Proteine des Speichels stimulieren diese selbst nicht, erfüllen aber unterschiedliche Aufgaben, die indirekt die Geschmackswahrnehmung beeinflussen. Dazu gehört neben Verdauungsenzymen wie der Amylase das Statherin, das für die niedrige Oberflächenspannung von Ruhe- und stimuliertem Speichel verantwortlich ist. Durch die niedrige Oberflächenspannung des Speichels wird die Interaktion der Geschmacksstoffe mit den Zellen der Geschmacksknospen erleichtert.
Der Ruhespeichel wird zu 60–70 % von den sublingualen und submandibulären Speicheldrüsen gebildet und ist reich an Glykoproteinen wie Mucin und IgA. Mucine sind nicht im stimulierten Speichel der Ohrspeicheldrüse enthalten und vermitteln die deutlich höhere Viskosität und Adhäsivität des Ruhespeichels, wodurch eine Schutzschicht für die Strukturen der Mundhöhle gebildet wird. Bei Patient:innen mit Xerostomie fehlt diese und führt daher zu Folgen wie Infektanfälligkeit, Kariesneigung, Mundbrennen oder Geschmacksstörung.
Im Rahmen der Sekretion des Speichels werden aus dem Primärspeichel Natrium- und Chlorid-Ionen rückresorbiert, womit die Wahrnehmungsschwelle von Salz vermindert wird und somit die Empfindlichkeit erhöht wird, da es an den Geschmacksknospen zu einer Adaptation der Geschmackszellen kommt. Außerdem hat der Ruhespeichel eine geringe Pufferkapazität (Bikarbonate und Carboanhydrase werden erst mit erhöhter Speichelflussrate erhöht), sodass die Wahrnehmungsschwelle für H+-Ionen, die den sauren Geschmack vermitteln, ebenfalls bei Stimulation geringer ist, wodurch die hohe Empfindlichkeit für den sauren Geschmack begründet ist.
Die Geschmackswahrnehmung ist als Nahsinn auf den direkten Kontakt der aufgenommenen Stoffe im Mund mit den Geschmackspapillen der Zunge angewiesen. Danach erfolgt die reflektorische Bewertung des Gehalts mit den unmittelbar nachfolgenden physiologischen Reaktionen. Durch deutlichen Zungenbelag oder Entzündungen kann dieser Prozess gestört sein.
Bitter hat eine wichtige Warnfunktion vor potenziell toxischen Stoffen (z. B. in verdorbenen Lebensmitteln) und kann zu unmittelbarem Ausspucken oder zu Erbrechen führen. Damit es auch bei vermindertem Schmeckvermögen zu einer ausreichenden Signalübertragung kommt, ist die redundante Versorgung der Zunge mittels doppelseitiger Innervation zweier Hirnnervenpaare so wichtig.
Der von vielen als angenehm empfundene Bittergeschmack bestimmter Lebensmittel (z. B. Kaffee, Bier, chininhaltige Getränke) wird erst durch Lernprozesse bzw. Gewöhnung erreicht. Studien mit Neugeborenen zeigten, dass Bitterstoffe zu unmittelbaren Abwehrreaktionen mit dem Ziel der Abwehr potenziell gesundheitsschädlicher Substanzen führen. In einem anderen Studiensetting wiesen Schwangere im ersten Trimenon eine erhöhte Empfindlichkeit für bitter auf. Dies könnte mit einem Schutz vor der Aufnahme potenziell giftiger Substanzen in der für die Entwicklung des Kindes besonders empfindlichen Phase in Zusammenhang stehen.
Details
- Seiten
- 128
- ISBN (ePUB)
- 9783991116295
- Sprache
- Deutsch
- Erscheinungsdatum
- 2022 (August)
- Schlagworte
- Schmecken Bertold Renner Riechstörungen Diagnose Christian A. Müller Riechverlust chemische Sinne Anamnese Therapie Riechen Anosmie Schmeckstörungen

